2026-03-24 22:16:13
上周醫藥生物指數跌1.38%,跑贏上證指數。BD收入成創新藥企重要資金來源,中國創新藥出海BD總包達571億美元。ELCC2026展現中國本土創新加速態勢。愛科百發三闖港股,稱無商業化產品,仍處虧損階段。上周國家藥監局披露108條臨床試驗登記信息,1款創新藥獲批。此外,三生制藥貧血新藥、恒瑞醫藥ADC藥物臨床研究有新進展。
每經記者|金喆 每經編輯|魏官紅
一周行情
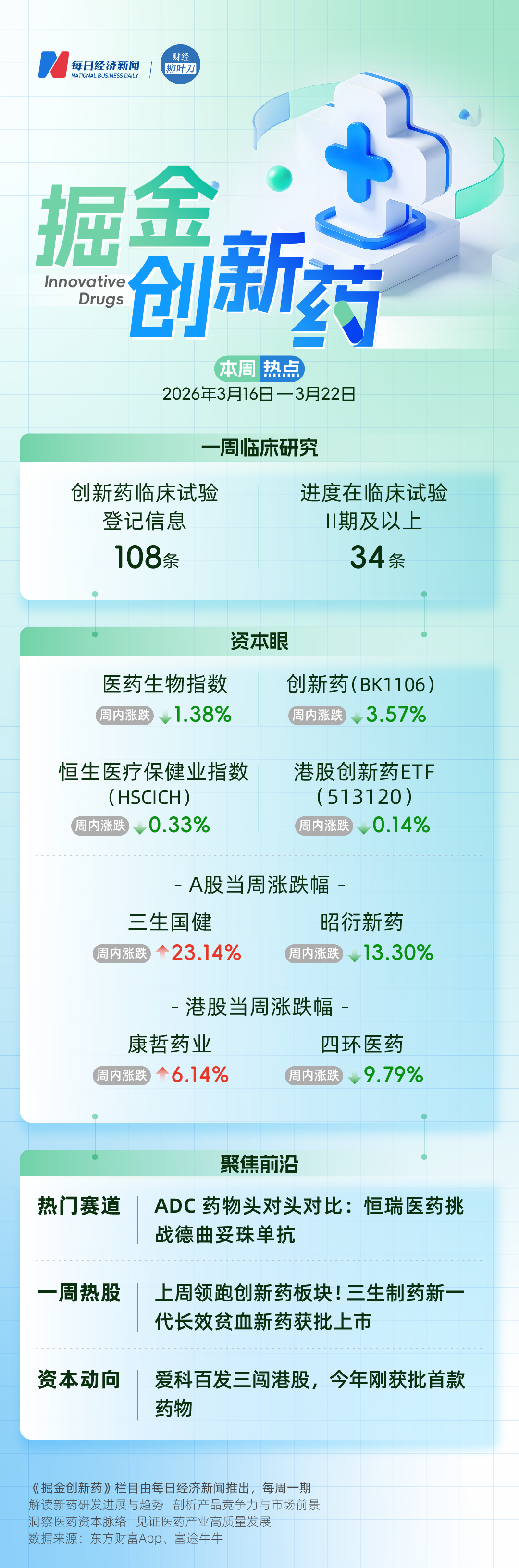
上周(3月16日至3月20日)醫藥生物指數下跌1.38%,跑贏上證指數2個百分點。創新藥(BK1106)周內下跌3.57%;恒生醫療保健業指數(HSCICH)周內下跌0.33%;港股創新藥ETF(513120)周內下跌0.14%。
一周點評
BD收入已經成為企業重要資金來源 長期看好創新藥產業發展邏輯
2026年中國創新藥出海BD(商務拓展)總包已經達571億美元,首付33億美元,數量達53件。BD收入已經成為中國創新藥企重要資金來源。東吳證券通過計算“現金及現金等價物/年研發費用”來評估創新藥板塊的資金面是否充裕。整體而言,當前醫藥板塊資金面充裕,絕大多數企業仍保持了1年以上的研發資金覆蓋能力,能夠有效支撐后續臨床試驗推進、管線拓展及技術創新,為行業長期高質量發展奠定了穩健的財務基礎,也為創新藥企業的技術突破與商業化轉化提供了充足的時間窗口。
ELCC2026再展現中國從“follow”到“First(FFBC)”的本土創新加速態勢
ELCC2026值得重點關注二代免疫聯合方案、單/雙抗ADC(Trop2、HER3等)、KRAS/HER2/EGFR等驅動基因靶向療法以及AI輔助診斷與個性化治療等方向。ELCC2026再次展現出中國從“follow”到“First(FFBC)”的本土創新加速態勢。科倫博泰sac-TMT入選LBA研究。
整體上,開源證券持續看好創新藥(886015)及其產業鏈(CXO+科研服務)及AI、腦機接口(886047)、生物制造等國家戰略性新興產業。即將迎來2026年第一季度業績期,創新產業鏈有望延續業績整體向上的趨勢,臨床前CRO簽單有望加速增長,當前位置重點推薦。
一周新股動向
愛科百發三闖港股 今年剛獲批首款藥物
3月17日,上海愛科百發生物醫藥技術股份有限公司(以下簡稱“愛科百發”)三度遞表港交所主板。
評估一家創新藥的價值,核心是看已上市產品的商業化表現和研發管線的進度和稀缺性。招股書顯示,愛科百發成立于2013年,已開發六種候選藥物的管線。其中兩項授權引進的產品,一款是2014年1月從羅氏公司獲得的呼吸道合胞病毒(RSV)藥物齊瑞索韋,已于2025年提交NDA(上市許可申請),針對1到24個月嬰幼兒RSV感染。
愛科百發表示,就RSV預防而言,帕利珠單抗、尼塞韋單抗及克萊羅韋單抗(全部均為預防性抗體)為目前全球僅有的三款獲批準用于預防RSV的藥物。然而,其僅獲批準用于預防少數具有特異性特征的嬰幼兒群體的RSV感染,在中國僅有尼塞韋單抗獲批準。截至最后實際可行日期,全球僅有五種RSV抗體處于臨床開發階段,包括愛科百發的AK0610。
為何會從羅氏引進該藥物?愛科百發表示,齊瑞索韋由公司創始人鄔博士于羅氏研發(中國)有限公司工作時共同發明。鄔博士離開羅氏研發(中國)有限公司后,創立了愛科百發,并就齊瑞索韋的授權許可安排與羅氏等相關方進行積極協商。
另一款是2018年從羅氏、基因泰克及Intermune引進的AK3280,這是一種處于II期后概念驗證臨床試驗階段的特發性肺纖維化(IPF)藥物。
對于IPF藥物的商業價值,愛科百發在招股書中提到,美國及中國目前僅有三種藥物獲批準用于治療IPF。相關藥物有若干臨床限制,有副作用可能導致治療中斷。
愛科百發還表示,截至報告披露日,公司沒有商業化產品。記者注意到,今年1月5日,愛科百發申報的絲右哌甲酯右哌甲酯復方膠囊(商品名:愛智達)獲批上市,用于治療6歲及6歲以上注意缺陷多動障礙(ADHD)。這是全球唯一速釋加緩釋復方制劑,是針對ADHD患者的Best-in-Class創新治療藥物。但獲批不到2個月,愛科百發就有新動作。3月3日,愛科百發與齊魯制藥達成4.7億元潛在總對價的合作,將愛智達(AK0901)在中國地區的商業化權利授予齊魯藥業。
但公司目前仍處于虧損階段。2024年和2025年,愛科百發其他收入及收益分別為2630.5萬元、757.4萬元,年內虧損分別為1.97億元、2.27億元。
根據醫藥魔方提供的數據,3月16日至3月20日,國家藥品監督管理局藥品審評中心共披露108條臨床試驗登記信息,其中34條為處于臨床試驗II期及以上的創新藥新登記臨床試驗信息,有3個臨床研究項目正在招募患者。

數據來源:醫藥魔方提供
上周,有1款創新藥獲批。

數據來源:醫藥魔方提供
三生制藥新一代長效貧血新藥獲批上市
3月19日,中國國家藥品監督管理局批準三生制藥1類生物創新藥羅賽促紅素α注射液(新比澳)上市,批準適應證為治療因慢性腎臟病引起的貧血且正在接受促紅細胞生成素治療的血液透析患者。這是公司在腎科治療領域的又一重要進展,為廣大患者帶來更多的選擇和獲益。
慢性腎臟病(CKD)相關貧血是透析患者最常見的并發癥之一,在晚期CKD人群中尤為普遍。其中,亞洲地區CKD患者貧血總體患病率約為42%,在CKD V期患者中可高達80%。隨著我國透析患者規模持續擴大,貧血管理的重要性不斷提升,已逐漸成為血液凈化質量控制的重要指標之一。
在治療策略方面,國內外多項指南均持續推薦促紅細胞生成刺激劑(ESAs)作為腎性貧血的一線治療藥物。從國際臨床實踐來看,長效ESAs的使用比例約50%,而我國治療結構仍以短效ESAs為主,這種方式下需頻繁注射,患者依從性低、醫療負擔沉重。因此,羅賽促紅素α注射液的上市為臨床治療結構的優化提供了新的可能。一項多中心、隨機、開放、陽性藥平行對照的III期研究納入300例接受血液透析的慢性腎衰竭貧血患者,受試者均在篩選期接受益比奧穩定治療至少12周,且血紅蛋白水平維持在100g/L~120g/L范圍內。
研究結果顯示,在評價期(第25周~32周),羅賽促紅素α注射液組與益比奧組平均Hb變化值分別為?1.460g/L與?1.582g/L,兩組差值95%置信區間為0.122(?1.819,2.063)g/L,其置信區間下限高于預設非劣效界值,提示羅賽促紅素α注射液在維持治療中的療效非劣于人促紅素注射液。同時,未觀察到新的安全性信號,整體安全性良好可控。
ADC藥物頭對頭對比:恒瑞醫藥挑戰德曲妥珠單抗
醫藥魔方數據庫顯示,3月20日,恒瑞醫藥登記一項臨床試驗,為“注射用瑞康曲妥珠單抗不同劑量或德曲妥珠單抗治療HR陽性HER2低表達的不可切除的局部復發/轉移性乳腺癌的隨機、開放、多中心II期臨床研究”。
每經記者注意到,該臨床試驗的主試驗藥物為注射用瑞康曲妥珠單抗是恒瑞醫藥自主研發的國產ADC,對照組藥物德曲妥珠單抗(T-DXd)是全球首個獲批HER2低表達適應證的ADC藥物,也是該治療領域的“金標準”。此次頭對頭研究可直接驗證國產藥物是否能達到進口藥療效,甚至在安全性(如肺毒性風險)上更優。
據了解,HER2低表達乳腺癌患者此前被歸為“HER2陰性”,占所有乳腺癌群體的45%~55%,此前長期面臨“治療空白”,只能依賴化療或內分泌治療,療效有限且副作用大。
若研究達到預期終點,將從三個層面改變臨床治療格局。
患者層面,新增“國產ADC”治療選擇,同時可能通過劑量優化減少副作用,提升治療耐受性和生活質量。
醫生層面,為臨床決策提供“頭對頭”證據,醫生可根據患者具體情況選擇更適配的ADC藥物,而非僅依賴單一進口藥。
行業層面,推動國產ADC藥物在細分領域的突破,為后續 HER2低表達、HER2零表達等更細分亞型的研究提供參考。
3月24日是世界防治結核病日,也是李語(化名)確診結核病的第40天。
當醫生指著X光片上肺部出現的幾個小空洞說出“結核病”的時候,李語感到很茫然,她甚至把結核病和塵肺搞混了:我沒有長期吸入粉塵顆粒,為什么會得這個病?
對于23歲的李語來說,結核病菌離自己很遙遠。在她還沒有出生的時候,這種一百多年前被發現的“結核分枝桿菌”,差點就被埋進歷史書里了——上世紀80年代,曾有科學家樂觀地預言,2000年人類會消滅結核病。
然而,由于耐藥菌株進化、預防性治療不足、缺乏突破性療法,世界衛生組織將“終結結核病流行”的時間推遲到了2035年,而這一目標很可能無法如期實現。
只有未來更靈敏的檢測工具或更有效的疫苗才能打破僵局嗎?多位業內人士告訴《每日經濟新聞》記者,他們不認同這一觀點。
如需轉載請與《每日經濟新聞》報社聯系。
未經《每日經濟新聞》報社授權,嚴禁轉載或鏡像,違者必究。
讀者熱線:4008890008
特別提醒:如果我們使用了您的圖片,請作者與本站聯系索取稿酬。如您不希望作品出現在本站,可聯系我們要求撤下您的作品。
歡迎關注每日經濟新聞APP
