2026-03-24 19:39:22
3月24日,復星醫(yī)藥(600196.SH;02196.HK)公布2025年度經(jīng)營業(yè)績。復星醫(yī)藥以創(chuàng)新研發(fā)突破與全球化體系升級為雙引擎,實現(xiàn)營業(yè)收入人民幣416.62億元,同比增長1.45%,其中,創(chuàng)新藥品收入98.93億元,同比增長29.59%;境外收入129.77億元,同比增長14.87%;歸母凈利潤33.71億元,同比增長21.69%;歸母扣非凈利潤23.40億元,同比增長1.12%;經(jīng)營活動產(chǎn)生的現(xiàn)金流量凈額為52.13億元,同比增長16.45%,高質(zhì)量發(fā)展底座進一步夯實。
2025年,復星醫(yī)藥創(chuàng)新藥品收入98.93億元,占制藥業(yè)務收入比重提升至33.16%,成為業(yè)績增長核心引擎。全年研發(fā)總投入共計59.13億元,同比增長6.46%,其中,創(chuàng)新藥品相關(guān)研發(fā)投入達43.03億元、同比增長15.98%,占制藥業(yè)務研發(fā)投入的80.26%。
高強度研發(fā)投入轉(zhuǎn)化為豐碩成果,報告期內(nèi),7個創(chuàng)新藥品共16項適應癥于境內(nèi)外獲批上市,6個創(chuàng)新藥品種上市申請獲受理,近40項創(chuàng)新藥臨床試驗獲中美歐批準,多個核心產(chǎn)品進入關(guān)鍵臨床階段,為后續(xù)商業(yè)化增長奠定堅實管線基礎(chǔ)。此外,有5款創(chuàng)新藥新納入2025年國家醫(yī)保目錄,CAR-T產(chǎn)品奕凱達(阿基侖賽注射液)納入首版商保創(chuàng)新藥目錄,在提升創(chuàng)新藥患者可及性的同時,進一步打開商業(yè)化放量空間。
復星醫(yī)藥以創(chuàng)新藥為發(fā)展重點,圍繞腫瘤(實體瘤、血液瘤)、免疫炎癥、神經(jīng)退行性疾病三大核心領(lǐng)域,通過自主研發(fā)、合作開發(fā)、許可引進等持續(xù)強化管線建設(shè)。
腫瘤領(lǐng)域:2025年,復星醫(yī)藥圍繞乳腺癌、肺癌等重點適應癥強化創(chuàng)新管線布局。自研小分子創(chuàng)新藥復邁寧(蘆沃美替尼片)雙適應癥國內(nèi)獲批,填補國內(nèi)罕見腫瘤治療空白; CDK4/6抑制劑復妥寧(枸櫞酸伏維西利膠囊)2項適應癥上市,為乳腺癌患者帶來全新治療選擇;抗PD-1單抗斯魯利單抗注射液在歐洲及多個新興市場獲批,成為首個在歐盟獲批用于一線治療廣泛期小細胞肺癌(ES-SCLC)的抗PD-1單抗;HLX43、HLX22等抗體/ADC藥物進入關(guān)鍵臨床階段,腫瘤管線梯隊持續(xù)完善。第二款CAR-T產(chǎn)品布瑞基奧侖賽上市申請獲受理。
免疫炎癥與慢病領(lǐng)域:許可引進的First-in-Class創(chuàng)新藥萬緹樂(鹽酸替那帕諾片)獲批上市,為中國慢性腎臟病透析患者提供全新治療方案;FXS7553等核心產(chǎn)品臨床進展穩(wěn)步推進。
神經(jīng)退行性疾病領(lǐng)域:帕金森病治療藥物奧吡卡朋膠囊通過“先行先試”在海南博鰲落地;復星醫(yī)視特加速“磁波刀”產(chǎn)品升級與適應癥拓展;將甘露特鈉膠囊納入阿爾茨海默病創(chuàng)新藥管線,并推進其上市后確證性臨床試驗;許可引進的AR1001進入全球多中心III期臨床。通過上述舉措,進一步豐富公司在神經(jīng)退行性疾病領(lǐng)域的產(chǎn)品管線布局。
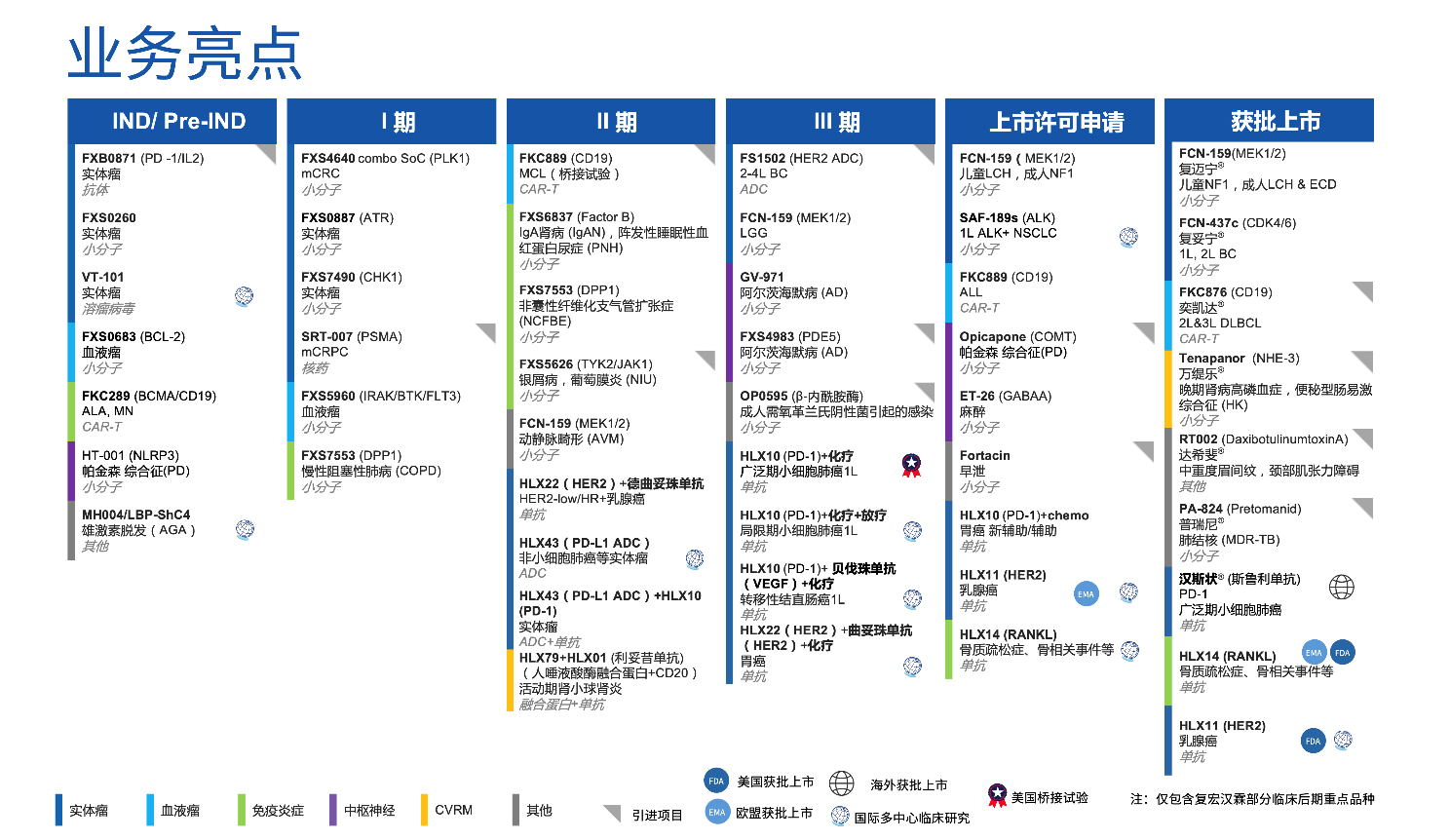
在夯實抗體和ADC、小分子、細胞治療等核心技術(shù)平臺的基礎(chǔ)上,復星醫(yī)藥前瞻性布局核藥、小核酸等前沿賽道,核藥項目SRT-007順利啟動I期臨床試驗,初步建立“影像診斷 - 靶向治療”的診療一體化研發(fā)路徑;細胞治療領(lǐng)域自體雙靶點CAR-T產(chǎn)品FKC289臨床試驗申請獲國家藥監(jiān)局受理,為后續(xù)創(chuàng)新產(chǎn)品儲備持續(xù)賦能。
2025年,復星醫(yī)藥全球化資源整合能力顯著增強,全年對外許可首付款總金額超2.6億美元,潛在里程碑總金額超38億美元。其中,GLP-1靶點YP05002全球許可項目首付款1.5億美元、潛在總金額20.85億美元,充分印證公司創(chuàng)新研發(fā)的全球競爭力。合作開發(fā)方面,復星醫(yī)藥與Teva聯(lián)合開發(fā)FXB0871;與Aditum Bio旗下基金建立源頭創(chuàng)新合作。與此同時,復星醫(yī)藥通過許可引進方式高效引入奧康澤、普瑞尼、達希斐等多款境外原研藥并實現(xiàn)中國境內(nèi)獲批上市。
2025年,復星醫(yī)藥的國際化進程實現(xiàn)從“產(chǎn)品出海”向“體系出海”的戰(zhàn)略升級,在創(chuàng)新研發(fā)、生產(chǎn)質(zhì)量、注冊準入、商業(yè)化及學術(shù)影響力等維度全面突破,構(gòu)建起覆蓋中國、美國、歐洲、非洲、印度及東南亞等市場的全球運營網(wǎng)絡。2025年,復星醫(yī)藥境外收入129.77億元,占營業(yè)收入31.15%,占比同比提升3.64個百分點。
復星醫(yī)藥已形成“歐美主導突破、新興市場深耕”的全球研產(chǎn)協(xié)同的注冊能力。核心品種斯魯利單抗注射液累計已在全球超過40個國家和地區(qū)獲批上市,聯(lián)合化療一線治療ES-SCLC的美國橋接試驗已完成患者入組,計劃2026年向FDA遞交相應生物制品許可申請(BLA);生物類似藥地舒單抗等產(chǎn)品相繼獲得美國FDA及歐盟批準,標志著生物藥平臺質(zhì)量體系與注冊能力獲國際標準認證;小分子創(chuàng)新藥復邁寧獲沙特阿拉伯"突破性療法"認定,成為撬動中東及全球市場的重要支點。
復星醫(yī)藥已有17個中國境內(nèi)車間/生產(chǎn)線通過美國、歐盟、WHO等主流法規(guī)市場GMP認證,生物藥產(chǎn)線已實現(xiàn)向中國、歐洲、拉美、東南亞、印度等市場常態(tài)化供貨;印度Gland Pharma多條注射劑產(chǎn)線通過歐美日澳認證,為全球供應鏈穩(wěn)定性與質(zhì)量可控性提供堅實保障。
復星醫(yī)藥已形成“自主運營+許可授權(quán)”雙軌并行的成熟出海模式,全球商業(yè)化團隊超6,000人,在非洲建立覆蓋40多個國家和地區(qū)的營銷網(wǎng)絡;控股子公司復銳醫(yī)療科技營銷網(wǎng)絡覆蓋超110個國家和地區(qū),博毅雅覆蓋超50個國家和地區(qū)。
在核心業(yè)務高質(zhì)量發(fā)展的同時,2025年,復星醫(yī)藥MSCI ESG評級提升至AA級,恒生ESG評級保持A-級,并入選2025《財富》中國ESG影響力榜單,成為該榜單唯一的中國醫(yī)藥企業(yè)。
復星醫(yī)藥董事長陳玉卿表示,2025年,復星醫(yī)藥堅定踐行“創(chuàng)新引領(lǐng)、深度國際化、全面擁抱 AI”的公司戰(zhàn)略,創(chuàng)新藥與全球化成驅(qū)動業(yè)績高質(zhì)量發(fā)展的雙引擎。展望未來,復星醫(yī)藥將始終聚焦未滿足臨床需求,持續(xù)創(chuàng)新,繼續(xù)深耕腫瘤、免疫炎癥、神經(jīng)退行性疾病等核心領(lǐng)域,以全球視野整合創(chuàng)新資源,以數(shù)字智能驅(qū)動運營升級,致力于成為全球領(lǐng)先的醫(yī)療創(chuàng)新整合者,為股東創(chuàng)造長期價值,為全球患者提供更多優(yōu)質(zhì)、可及的醫(yī)療健康解決方案。
(本文不構(gòu)成任何投資建議,信息披露內(nèi)容以公司公告為準。投資者據(jù)此操作,風險自擔。)
特別提醒:如果我們使用了您的圖片,請作者與本站聯(lián)系索取稿酬。如您不希望作品出現(xiàn)在本站,可聯(lián)系我們要求撤下您的作品。
歡迎關(guān)注每日經(jīng)濟新聞APP
